受理號(hào):CQZ2100988
醫(yī)療器械產(chǎn)品注冊(cè)技術(shù)審評(píng)報(bào)告
產(chǎn)品中文名稱(chēng):膝關(guān)節(jié)置換手術(shù)導(dǎo)航定位系統(tǒng)?
產(chǎn)品管理類(lèi)別:第三類(lèi)?
申請(qǐng)人名稱(chēng):蘇州微創(chuàng)暢行機(jī)器人有限公司
國(guó)家藥品監(jiān)督管理局?
醫(yī)療器械技術(shù)審評(píng)中心
基本信息?
一、申請(qǐng)人名稱(chēng)?蘇州微創(chuàng)暢行機(jī)器人有限公司?
二、申請(qǐng)人住所 蘇州工業(yè)園區(qū)鳳里街 151 號(hào) 3 號(hào)廠房部分區(qū)域?
三、生產(chǎn)地址 蘇州工業(yè)園區(qū)鳳里街 151 號(hào) 3 號(hào)廠房 3 層 A 區(qū)
技術(shù)審評(píng)概述?
(一)產(chǎn)品結(jié)構(gòu)及組成?
該產(chǎn)品由導(dǎo)航控制臺(tái)(導(dǎo)航臺(tái)車(chē)、光學(xué)導(dǎo)航設(shè)備、顯示器)、 手術(shù)平臺(tái)(機(jī)械臂、手術(shù)臺(tái)車(chē))、手術(shù)輔助工具、光學(xué)定位標(biāo)記、 腳踏開(kāi)關(guān)和線纜組成。?
(二)產(chǎn)品適用范圍 該產(chǎn)品與經(jīng)驗(yàn)證的膝關(guān)節(jié)假體聯(lián)合使用,在成人全膝關(guān)節(jié) 置換手術(shù)中,用于膝關(guān)節(jié)假體和手術(shù)工具的導(dǎo)航定位。?
(三)型號(hào)/規(guī)格 OSR-1000?
(四)工作原理 該產(chǎn)品工作原理為術(shù)前規(guī)劃及術(shù)中定位。即術(shù)者在術(shù)前基 于患者情況及術(shù)前 CT 圖像完成術(shù)前規(guī)劃。術(shù)中基于光學(xué)導(dǎo)航系 統(tǒng)反饋的實(shí)時(shí)臨床參數(shù)完成術(shù)中評(píng)估并調(diào)整術(shù)前規(guī)劃,隨后機(jī) 械臂在光學(xué)導(dǎo)航系統(tǒng)輔助下完成截骨面定位,術(shù)者通過(guò)機(jī)械臂 輔助完成截骨。?
該產(chǎn)品性能指標(biāo)包括物理性能、軟件功能(導(dǎo)航軟件、控 制軟件、使用限制)、操作性能(系統(tǒng)定位精度(位置重復(fù)性、 姿態(tài)重復(fù)性和距離準(zhǔn)確性)、系統(tǒng)精度(位置準(zhǔn)確度和姿態(tài)準(zhǔn)確 度)、機(jī)械臂各軸運(yùn)動(dòng)范圍、機(jī)械臂末端啟動(dòng)力、工作空間范圍、 靶標(biāo)跟蹤響應(yīng)時(shí)間、故障響應(yīng)時(shí)間、臺(tái)車(chē)移動(dòng)力、臺(tái)車(chē)鎖緊力、 機(jī)械臂保持力、機(jī)械臂滿載的偏移量、機(jī)械臂抱閘鎖緊力、噪 聲、刷新率、最大追蹤數(shù)量)、網(wǎng)絡(luò)安全、光學(xué)定位標(biāo)記、手術(shù) 輔助工具、報(bào)警要求、腳踏性能、電氣安全、電磁兼容性等。?
申請(qǐng)人針對(duì)上述性能指標(biāo)提交了產(chǎn)品性能研究資料,同時(shí) 提交了產(chǎn)品技術(shù)要求與檢測(cè)報(bào)告,檢測(cè)結(jié)果與產(chǎn)品技術(shù)要求相符。?
該產(chǎn)品所含手術(shù)輔助工具中截骨板、部分靶標(biāo)支架頭端、 固定針固定組件、靶標(biāo)固定螺桿、靶標(biāo)固定轉(zhuǎn)體、擰緊把手、 固定針安裝導(dǎo)向器、固定針、骨定位針、滑車(chē)平面定位片、旋 擰壓緊柱與人體骨/組織短期接觸;光學(xué)定位標(biāo)記存在脫落風(fēng)險(xiǎn), 按照與骨/組織短期接觸進(jìn)行評(píng)價(jià)。?
申請(qǐng)人根據(jù) GB/T 16886.1-2011《醫(yī)療器械生物學(xué)評(píng)價(jià) 第 1 部分:風(fēng)險(xiǎn)管理過(guò)程中的評(píng)價(jià)與試驗(yàn)》進(jìn)行了生物相容性評(píng)價(jià), 證明產(chǎn)品生物相容性風(fēng)險(xiǎn)可接受。
光學(xué)定位標(biāo)記以無(wú)菌狀態(tài)提供,采用輻照滅菌。申請(qǐng)人提 交了滅菌過(guò)程確認(rèn)報(bào)告,證實(shí)產(chǎn)品無(wú)菌保證水平(SAL)滿足 要求。?
手術(shù)輔助工具使用前由終端用戶進(jìn)行滅菌。申請(qǐng)人提交了 滅菌研究資料,符合要求。?
申請(qǐng)人提供了光學(xué)定位標(biāo)記的有效期研究資料,通過(guò)加速 老化試驗(yàn)確定產(chǎn)品有效期,其貨架有效期為 0.5 年。?
依據(jù)《有源醫(yī)療器械使用期限指導(dǎo)原則》提交了產(chǎn)品穩(wěn)定 性研究資料。通過(guò)老化測(cè)試和關(guān)鍵部件的壽命測(cè)試分析等方法 確認(rèn)了產(chǎn)品的使用期限,該產(chǎn)品使用期限為 7 年。?
申請(qǐng)人提供了光學(xué)定位標(biāo)記無(wú)菌初包裝的確認(rèn)資料,并提 交了產(chǎn)品運(yùn)輸包裝驗(yàn)證報(bào)告,證實(shí)包裝完整性符合設(shè)計(jì)要求。?
該產(chǎn)品軟件包括運(yùn)動(dòng)控制軟件、電源板嵌入式軟件、手術(shù) 導(dǎo)航軟件,軟件安全級(jí)別均為 C 級(jí),發(fā)布版本均為 1,運(yùn)動(dòng)控 制軟件完整版本為 1.3.0.1,電源板嵌入式軟件完整版本為 1.1.1.1,手術(shù)導(dǎo)航軟件完整版本為 1.3.0.10;申請(qǐng)人按照《醫(yī)療 器械軟件注冊(cè)技術(shù)審查指導(dǎo)原則》提交了相應(yīng)級(jí)別的軟件描述文檔和軟件版本命名規(guī)則真實(shí)性聲明,證實(shí)該產(chǎn)品軟件設(shè)計(jì)開(kāi) 發(fā)過(guò)程規(guī)范可控,綜合剩余風(fēng)險(xiǎn)均可接受。?
申請(qǐng)人根據(jù)《醫(yī)療器械網(wǎng)絡(luò)安全注冊(cè)技術(shù)審查指導(dǎo)原則》 要求,提交了網(wǎng)絡(luò)安全描述文檔,證明該產(chǎn)品現(xiàn)有網(wǎng)絡(luò)安全風(fēng) 險(xiǎn)可控,已建立網(wǎng)絡(luò)安全應(yīng)急響應(yīng)預(yù)案。?
該產(chǎn)品符合以下安全性標(biāo)準(zhǔn):?
GB 9706.1-2007 《醫(yī)用電氣設(shè)備 第 1 部分:安全通用要求》?
GB 9706.15-2008《醫(yī)用電氣設(shè)備 第 1-1 部分:安全通用要 求 并列標(biāo)準(zhǔn):醫(yī)用電氣系統(tǒng)安全要求》?
YY 0505-2012 《醫(yī)用電氣設(shè)備 第 1-2 部分:安全通用要 求并列標(biāo)準(zhǔn):電磁兼容要求和試驗(yàn)》?
YY 0709-2009 《醫(yī)用電氣設(shè)備 第 1-8 部分:安全通用要 求 并列標(biāo)準(zhǔn):通用要求,醫(yī)用電氣設(shè)備和醫(yī)用電氣系統(tǒng)中報(bào)警 系統(tǒng)的測(cè)試和指南》?
YY 1057-2016 《醫(yī)用腳踏開(kāi)關(guān)通用技術(shù)條件》 申請(qǐng)人提交了相應(yīng)檢測(cè)報(bào)告,證實(shí)該產(chǎn)品符合上述標(biāo)準(zhǔn)要 求。?
申請(qǐng)人通過(guò)臨床試驗(yàn)路徑開(kāi)展臨床評(píng)價(jià)。該項(xiàng)研究采用前 瞻性、多中心、單組目標(biāo)值設(shè)計(jì),在五家醫(yī)療機(jī)構(gòu)開(kāi)展臨床試驗(yàn)。?
該項(xiàng)研究入組 106 例,以臨床成功率(即術(shù)后出院前下肢 力線與預(yù)期規(guī)劃偏移的角度≤ 3°臨床成功的例數(shù)占完成手術(shù)例 數(shù)的百分比)為主要評(píng)價(jià)指標(biāo);股骨遠(yuǎn)端外側(cè)角、脛骨近端內(nèi) 側(cè)角、KSS 評(píng)分(治療后與基線差值)、WOMAC 評(píng)分(治療后 與基線差值)為次要評(píng)價(jià)指標(biāo);研究期間發(fā)生的所有不良事件 及術(shù)后植入關(guān)節(jié)假體的位置情況作為安全性評(píng)價(jià)指標(biāo)。?
主要評(píng)價(jià)指標(biāo),F(xiàn)AS 集 106 例,臨床成功 105(99.06%)例;PPS 集 105 例,臨床成功 104(99.05%)例。FAS 集與 PPS 集中, 臨床成功率的 95%可信區(qū)間分別為[94.86%,99.98%][94.81%, 99.98%]。下限均大于目標(biāo)值 89%,臨床試驗(yàn)結(jié)論成立。?
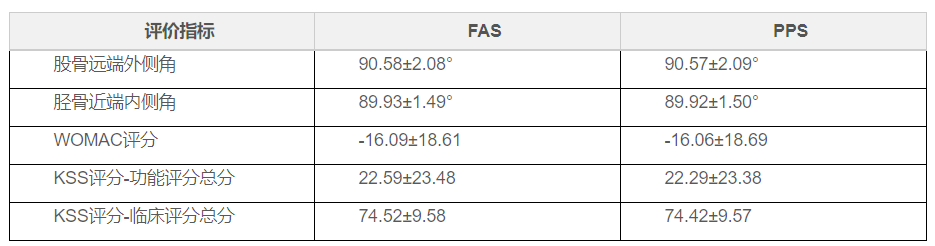
次要評(píng)價(jià)指標(biāo)結(jié)果如表所示
安全性評(píng)價(jià)指標(biāo):SS 集 106 例受試者,不良事件發(fā)生率 50.94%,嚴(yán)重不良事件發(fā)生率 3.77%,均判定與申報(bào)產(chǎn)品無(wú)關(guān)。臨床試驗(yàn)中未發(fā)生器械缺陷。?
四、產(chǎn)品受益風(fēng)險(xiǎn)判定?
該產(chǎn)品主要受益為:與經(jīng)驗(yàn)證的膝關(guān)節(jié)假體聯(lián)合使用,在 成人全膝關(guān)節(jié)置換手術(shù)中,用于膝關(guān)節(jié)假體和手術(shù)工具的導(dǎo)航 定位,并可降低患者和醫(yī)師的 X 射線輻射風(fēng)險(xiǎn)。?
(二)風(fēng)險(xiǎn)評(píng)估?
該產(chǎn)品主要風(fēng)險(xiǎn)為:?
1.光學(xué)定位系統(tǒng)受到遮擋無(wú)法定位的風(fēng)險(xiǎn),通過(guò)軟件提示、 用戶培訓(xùn)進(jìn)行風(fēng)險(xiǎn)控制。?
2.機(jī)械臂非預(yù)期運(yùn)動(dòng)的風(fēng)險(xiǎn),通過(guò)優(yōu)化設(shè)計(jì)進(jìn)行風(fēng)險(xiǎn)控制。
3.一次性使用器械未按要求一次性使用,重復(fù)性使用器械滅 菌不徹底,未按照說(shuō)明書(shū)進(jìn)行清潔消毒等,造成交叉感染,通 過(guò)用戶培訓(xùn)進(jìn)行風(fēng)險(xiǎn)控制。?
4.用戶操作不規(guī)范導(dǎo)致的風(fēng)險(xiǎn),通過(guò)用戶培訓(xùn)進(jìn)行風(fēng)險(xiǎn)控 制。上述風(fēng)險(xiǎn)均在說(shuō)明書(shū)中予以提示。
任何具有不適宜采用傳統(tǒng)膝關(guān)節(jié)置換手術(shù)的相對(duì)或絕對(duì)禁 忌癥患者,同樣不適用于采用膝關(guān)節(jié)置換手術(shù)導(dǎo)航定位系統(tǒng)輔 助膝關(guān)節(jié)置換手術(shù)。?
微創(chuàng)膝關(guān)節(jié)置換手術(shù)導(dǎo)航定位系統(tǒng)的患者選擇應(yīng)該基于手 術(shù)醫(yī)師對(duì)患者具體情況的判斷,在準(zhǔn)備行導(dǎo)航輔助 TKA 前,手 術(shù)醫(yī)師應(yīng)考慮下述情況:?
1.髖關(guān)節(jié)連接的完整性是完成骨注冊(cè)的必要條件;?
2.手術(shù)區(qū)域附近的金屬物品會(huì)影響 CT 掃描的質(zhì)量,進(jìn)而影 響手術(shù)規(guī)劃的精度;?
3.伴有感染或近期感染的患者不適合手術(shù);?
4.嚴(yán)重骨質(zhì)疏松的患者會(huì)影響假體穩(wěn)定性;?
5.患者體型會(huì)影響手術(shù)復(fù)雜性,術(shù)前應(yīng)評(píng)估患者 BMI;?
6.韌帶結(jié)構(gòu)缺失或不穩(wěn)可能會(huì)影響術(shù)后關(guān)節(jié)穩(wěn)定性;
7.顯著的畸形(如屈曲攣縮、固定膝內(nèi)外翻等)對(duì)手術(shù)的影響應(yīng)被仔細(xì)評(píng)估;?
8.無(wú)法使用指定全膝關(guān)節(jié)置換系統(tǒng)進(jìn)行手術(shù)的患者不能使 用本系統(tǒng)進(jìn)行手術(shù);?
9.其他醫(yī)生認(rèn)為可能影響手術(shù)正常進(jìn)行的因素。?
綜上,根據(jù)申請(qǐng)人提供的申報(bào)資料,經(jīng)綜合評(píng)價(jià),在目前 認(rèn)知水平上,產(chǎn)品臨床受益大于風(fēng)險(xiǎn)。
綜合評(píng)價(jià)意見(jiàn)?
注冊(cè)申請(qǐng)人申請(qǐng)境內(nèi)第三類(lèi)醫(yī)療器械注冊(cè),該申請(qǐng)項(xiàng)目適 用于創(chuàng)新醫(yī)療器械特別審查程序(受理號(hào):CQTS2000027), 提供的產(chǎn)品注冊(cè)申請(qǐng)資料齊全。依據(jù)《醫(yī)療器械監(jiān)督管理?xiàng)l例》(國(guó)務(wù)院令第 680 號(hào))、 《醫(yī)療器械注冊(cè)管理辦法》(國(guó)家食品藥品監(jiān)督管理總局令 2014 年第 4 號(hào))等相關(guān)醫(yī)療器械法規(guī)和配套規(guī)章,經(jīng)系統(tǒng)評(píng) 價(jià)注冊(cè)申請(qǐng)資料后,在目前認(rèn)知水平上,該產(chǎn)品上市帶來(lái)的受 益大于風(fēng)險(xiǎn),符合現(xiàn)行的技術(shù)審評(píng)要求,建議予以注冊(cè)。?
2022 年 4 月 18 日