? ? ? ?依據(jù)國家藥品監(jiān)督管理局《創(chuàng)新醫(yī)療器械特別審查程序》(國家藥監(jiān)局2018年第83號公告)要求,創(chuàng)新醫(yī)療器械審查辦公室組織有關(guān)專家對創(chuàng)新醫(yī)療器械特別審查申請進行了審查,擬同意以下申請項目進入特別審查程序,現(xiàn)予以公示。
1.產(chǎn)品名稱:靜脈支架系統(tǒng)
2.產(chǎn)品名稱:明膠-聚己內(nèi)酯分層牙齦修復(fù)膜
申 請 人:諾一邁爾(蘇州)醫(yī)學科技有限公司
3.產(chǎn)品名稱:經(jīng)導(dǎo)管二尖瓣置換系統(tǒng)
4.產(chǎn)品名稱:腦保護裝置系統(tǒng)
5.產(chǎn)品名稱:經(jīng)導(dǎo)管三尖瓣夾
6.產(chǎn)品名稱:主動脈弓支架系統(tǒng)
8.產(chǎn)品名稱:心臟冷凍消融系統(tǒng)
申 請 人:心諾普醫(yī)療技術(shù)(北京)有限公司
9.產(chǎn)品名稱:X射線計算機體層攝影設(shè)備?
申 請 人:Siemens Healthcare GmbH
公示時間:2022年9月28日至2022年10月17日
公示期內(nèi),任何單位和個人有異議的,可以書面、電話、郵件等方式向我中心綜合業(yè)務(wù)部反映。
電子郵箱:gcdivision@cmde.org.cn
特別說明:進入創(chuàng)新審查程序不代表已認定產(chǎn)品具備可獲準注冊的安全有效性,申請人仍需按照有關(guān)要求開展研發(fā)及提出注冊申請,藥品監(jiān)督管理部門及相關(guān)技術(shù)機構(gòu)將按照早期介入、專人負責、科學審查的原則,在標準不降低、程序不減少的前提下進行審評審批。
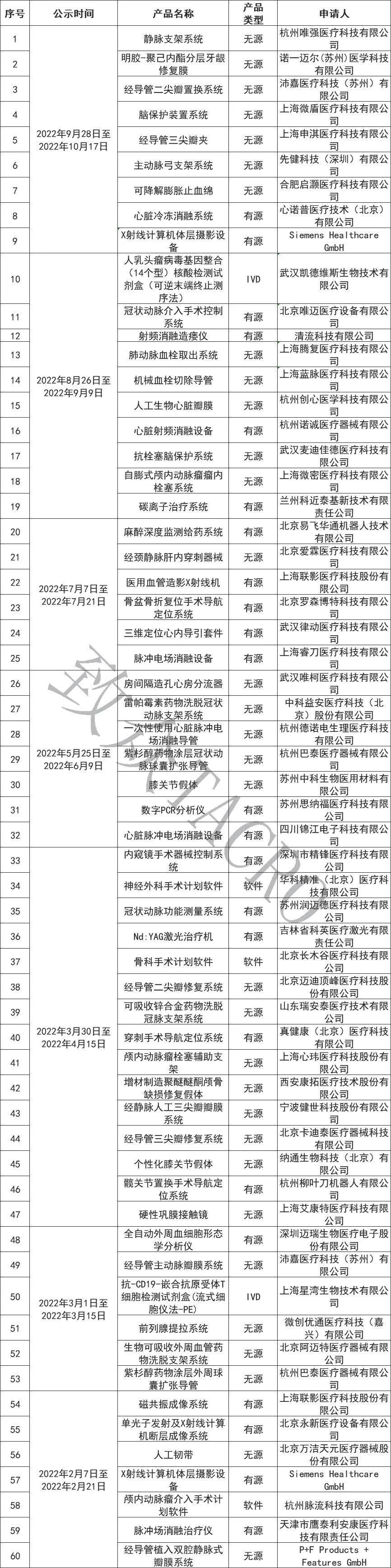
2022年所有進入創(chuàng)新特別審批的產(chǎn)品如下(點擊查看大圖):