受理號:CQZ1900597
醫療器械產品注冊技術審評報告?
國家藥品監督管理局?
醫療器械技術審評中心
基本信息?
二、申請人住所 武漢市東湖新技術開發區高新大道 818 號高科醫療器械園 B 區 12 號樓 4 層 2 號?
三、生產地址 武漢市東湖新技術開發區高新大道 818 號高科醫療器械園 B 區 12 號樓 4 層 2 號
技術審評概述?
產品由絲素蛋白、甘油和水組成。為兩面異性的單層結 構,上表面(光滑平整面)為平滑結構,肉眼可見標記“UP”字 樣,下表面(多孔褶皺面)為粗糙結構,無“UP”標記。產品經 環氧乙烷滅菌,以無菌方式提供。一次性使用。產品貨架有效 期 2 年。?
可吸收絲素修復膜需配合骨粉使用,作為物理屏障用于成 人患者拔牙后的拔牙窩位點保存。(三)型號/規格?
厚 度為 0.5±0.2mm ,規 格為 15mm×15mm 、 15mm×20mm、 20mm×30mm、25mm×30mm、30mm×40mm。?
(四)工作原理 作為物理屏障用于成人患者拔牙后的拔牙窩位點保存,需 配合骨粉使用。?
-
產品技術要求研究 產品技術要求研究項目如表 1 所示。
表 1 產品技術要求研究項目
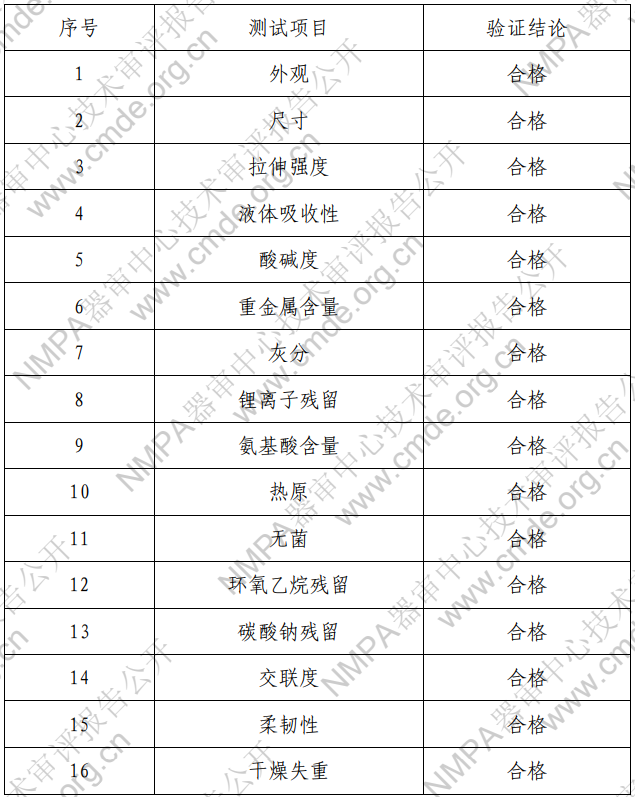
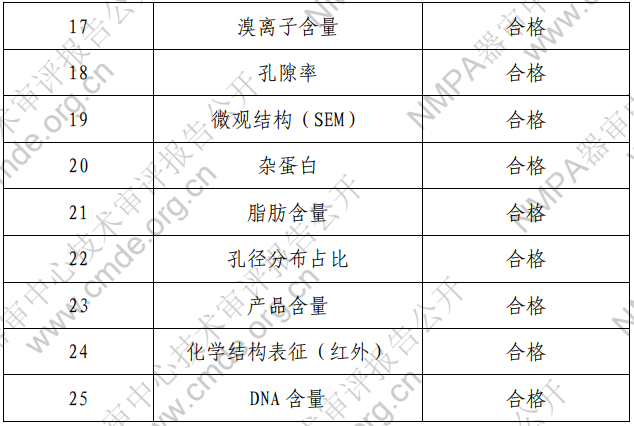
產品性能評價包括:外觀、尺寸、拉伸強度、液體吸收性、 酸堿度、重金屬含量、灰分、鋰離子殘留、氨基酸含量、熱原、 無菌、環氧乙烷殘留、碳酸鈉殘留、交聯度、柔韌性、干燥失重、 溴離子含量、孔隙率、微觀結構(SEM)、雜蛋白、脂肪含量、 孔徑分布占比、產品含量、化學結構表征(紅外)、DNA 含量、 吸收降解性能研究。?
該產品為植入器械,與組織持久接觸(>30 天)。申請人 依據 GB/T 16886 系列標準、YY/T 0268 標準和 ISO 10993 系列 標準進行了生物相容性評價,生物相容性風險可接受。
該產品原料為削口蠶繭,申請人依據《動物源性醫療器械產 品注冊申報資料指導原則》和 YY/T 0771 動物源醫療器械系列 標準,提供生物安全性研究資料。申請人從原材料供應商控制、 運輸和生產制造過程進行風險管理,對病毒去除/滅活、免疫原 性、產品免疫毒性進行研究。生物安全性研究資料顯示產品的 原料控制、病毒滅活、免疫原性和免疫毒性方面的風險可接受。
該產品采用環氧乙烷滅菌,無菌狀態提供。申請人提供了滅 菌確認報告,證明無菌保證水平可達 10-6。環氧乙烷殘留量不大 于 10μg/g。?
該產品貨架有效期為兩年。申請人提供了貨架有效期驗證 報告,驗證方式為加速老化和實時老化驗證,包括產品穩定性、 包裝完整性和運輸模擬驗證資料。?
申請人開展了動物試驗研究,通過日本大耳白兔口腔上顎 粘膜瓣缺損模型、動物有效性和安全性研究和比格犬體內屏障 膜作用研究,評價可吸收絲素修復膜在下頜骨硬組織修復治療 中的安全性和有效性。研究結果表明,可吸收絲素修復膜與對照組均具有屏障膜的作用,屏障膜作用無明顯差異。?
本次申報通過臨床試驗路徑開展臨床評價,采用前瞻性、多 中心、隨機、非劣效平行對照的設計,對照組為已上市的可吸收 生物膜,樣本量為 130 例(試驗組、對照組 1:1)。選擇手術后 7 天和 4 個月治療區域的牙槽骨高度和寬度的變化值為主要評 價指標,以牙周探診深度為次要有效性指標,安全性指標為術 后軟組織形態學檢查、術后生命體征檢查、實驗室檢查、器械缺 陷、合并用藥、不良事件及嚴重不良事件。?
臨床試驗結果顯示,術后 4 個月和術后 7 天的牙槽嵴高度 變化值,試驗組為0.97±0.25mm,對照組為 0.97±0.21mm, 兩組均數差值的95%置信區間(mm)95%CI為-0.082-0.081, 其上限小于非劣效界值 0.154;兩組術后 4 個月和術后 7 天的 牙槽嵴寬度變化值,試驗組為 0.96±0.24mm,對照組為 0.96± 0.24mm,兩組均數差值的 95%置信區間(mm)(不含交互項)中, 95%CI 為-0.080-0.088,其上限小于非劣效界值 0.184。次要指 標及安全性指標組間無統計學差異。
綜上,臨床試驗主要評價 指標非劣效假設成立。臨床評價資料符合技術審評要求。?
(一)該產品臨床使用可能為適用人群帶來的主要風險為:
2.用戶使用不規范導致的風險產品在某些非預期情況下, 如未經過專業培訓的使用者操作、可能會因使用操作錯誤導致 發生治療錯誤的風險。?
(二)根據申請人提供的申報資料,經綜合評價,在目前認 知水平上,認為該產品的上市為適用人群帶來的受益大于風險。為保證用械安全,在說明書中明示了相應警示及注意事項。
綜合評價意見?
本申報產品屬于同類首個醫療器械(受理編號:CQZ1900597)。申請人的注冊申報資料符合現行要求,依據《醫療器械監督管理條例》(國務院令第739號)、醫療器械注冊與備案管理辦法》(國家市場監督管理總局令第47號)等相關醫療器械法規與配套規章,經系統評價后,建議準予注冊。
2022 年 10 月 9 日
